Нейроэндокринные опухоли – это гетерогенная группа новообразований, источником которых являются нейроэндокринные клетки, в большом количестве рассредоточенные по всему организму. Терминологически объединены названием APUD-система (Amine Precursor Uptake and Decarboxylation, апудоциты - клетки, которые поглощают аминокислоты-предшественники с помощью реакции декарбоксилирования). Апудоциты являются эндокриноподобными клетками и располагаются в различных органах и тканях, при этом они могут быть одиночными или формировать небольшие скопления. Известно около 60 разновидностей клеток APUD-системы.
Функцией апудоцитов является образование биологически активных веществ посредством отщепления от аминокислот-предшественников карбоксильной группы (-COOH) и превращение их тем самым в амины или низкомолекулярные пептиды, поэтому характерным для нейроэндокринных опухолей является их способность продуцировать пептиды в избыточном количестве, что сопровождается появлением типичных гормональных синдромов.
Нейроэндокринные опухоли обычно характеризуются относительно медленным ростом, хотя и обладают злокачественным потенциалом. Встречаются случаи агрессивного и быстрого роста, а также случаи резистентности к лечению.
Для термина «нейроэндокринные опухоли» существуют различные синонимы, из которых в современной литературе наиболее распространенными являются «карциноид» (в настоящее время термин сохранен для нейроэндокринных опухолей легких, бронхов, червеобразного отростка) и «нейроэндокринная карцинома».
Нейроэндокринные опухоли могут быть самостоятельным заболеванием либо, некоторых случаях, являться частью синдрома множественной эндокринной неоплазии (МЭН), и необходимо дифференцировать два этих состояния, поскольку от этого зависит прогноз и выбор метода лечения. Синдром множественной эндокринной неоплазии может проявляться в двух вариантах:
- Синдром МЭН-1 (синдром Вермера) – наследственная патология, сопровождающаяся избыточным неконтролируемым ростом апудоцитов и обязательным поражением триады органов: гиперплазия или опухоли паращитовидных желез, нейроэндокринные опухоли поджелудочной железы и передней доли гипофиза. Также могут поражаться ДПК, желудок, тимус, легкие, щитовидная железа, надпочечники.
- Синдром МЭН-2 (2А) (синдром Сипла) - наследственная патология, проявляющаяся совместным развитием феохромоцитомы (гормонпродуцирующая опухоль надпочечника), медуллярного рака щитовидной железы и гиперплазией паращитовидных желез.
- Синдром МЭН-3 (2В) - наследственная патология, проявляющаяся совместным развитием феохромоцитомы, медуллярного рака щитовидной железы, гиперпаратиреозом и множественными невромами слизистых оболочек.
В последние 30 лет отмечается рост заболеваемости нейроэндокринными опухолями всех локализаций, и зачастую они диагностируются на распространенных стадиях. Чаще всего встречаются нейроэндокринные опухоли ЖКТ (около 66% среди нейроэндокринных опухолей и около 2% среди всех злокачественных опухолей ЖКТ), среди них преобладают опухоли слепой и прямой кишки. На втором месте по частоте встречаемости располагаются карциноиды в бронхолегочной системе (около 30% среди нейроэндокринных опухолей).
Классификация нейроэндокринных опухолей
По локализации апудоцитов, являющихся источников развития опухоли, нейроэндокринные опухоли можно классифицировать следующим образом:
- Нейроэндокринные опухоли (карциноиды) желудочно-кишечного тракта (ЖКТ).
- Нейроэндокринные опухоли (карциноиды) легкого.
- Новообразования эндокринных клеток желез внутренней секреции:
- Медуллярный рак щитовидной железы.
- Опухоли паращитовидных желез.
- Феохромоцитома (гормонально-активная опухоль надпочечников).
- Опухоли гипофиза.
- Карцинома Меркеля – злокачественная опухоль из клеток кожи, обеспечивающих тактильную чувствительность.
- Опухоли других локализаций (опухоли молочной железы, простаты, почек, яичников, тимуса)
Согласно более старой, но использующейся до настоящего времени классификации, нейроэндокринные опухоли делятся в зависимости от отдела первичной кишки, из клеток которой возникло новообразование (эмбриологическая классификация):
- Переднекишечный тип (Foregut), к которому относятся нейроэндокринные опухоли следующих локализаций:
- Тимус.
- Легкое.
- Бронхи.
- Пищевод.
- Желудок.
- Поджелудочная железа.
- Проксимальный отдел двенадцатиперстной кишки (ДПК).
- Среднекишечный тип (Midgut):
- a. Дистальная часть ДПК.
- b. Тонкая кишка.
- c. Проксимальные отделы толстой кишки (аппендикс, слепая кишка, восходящая и поперечная ободочная).
- Заднекишечный тип (Hingout):
- Дистальная часть толстой кишки (нисходящая ободочная и сигмовидная).
- Прямая кишка.
Всемирной организацией здравоохранения (ВОЗ) предложена единая классификация для нейроэндокринных опухолей ЖКТ независимо от их локализации:
- Высокодифференцированные нейроэндокринные опухоли с «доброкачественным» биологическим поведением или с неопределенным потенциалом злокачественности.
- Высокодифференцированные нейроэндокринные карциномы низкой степени злокачественности.
- Низкодифференцированные нейроэндокринные карциномы высокой степени злокачественности; к ним относятся крупноклеточные эндокринные и мелкоклеточные карциномы.
Классификация ВОЗ опухолей легких выделяет следующие гистологические виды:
- «Типичный» карциноид низкой степени злокачественности).
- «Атипичный» карциноид (промежуточной степени злокачественности)
- Крупноклеточная нейроэндокринная карцинома
- Мелкоклеточный рак легкого.
Следует отметить, что крупноклеточная нейроэндокринная карцинома и мелкоклеточный рак легкого не относятся к категории карциноидов и являются низкодифференцированными раками высокой степени злокачественности, при этом крупноклеточная нейроэндокринная карцинома рассматривается как подгруппа крупноклеточных карцином, а мелкоклеточный рак легкого является независимой нозологической единицей.
Также ВОЗ разработаны специальные классификации для конкретных локализаций, основанные на наиболее значимых прогностических факторах, к которым относятся глубина инвазии опухоли, наличие метастазов, размер первичной опухоли, поражение кровеносных и лимфатических сосудов, нейроинвазия, митотическая активность и содержание маркера клеточной пролиферации Ki-67.
Кроме того, для различных локализаций нейроэндокринных опухолей разработаны классификации TNM, основанные на размере опухоли, степени ее распространения поражении регионарных лимфатических узлов и наличии отдаленных метастазов.
Симптомы нейроэндокринных опухолей
Нейроэндокринные опухоли могут быть как функционирующими (сопровождающимися появлением специфических симптомов и синдромов), так и нефункционирующими. Нефункционирующие опухоли обычно обнаруживаются на более поздних стадиях, чем функционирующие.
Клиническим проявлением нейроэндокринных опухолей является так называемый карциноидный синдром, наиболее тяжелым и в некоторых случаях жизнеугрожающим осложнением которого является карциноидный криз, то есть резкое ухудшение состояния пациента, связанное с функционированием опухоли. Криз может возникнуть спонтанно или же быть спровоцированным такими факторами, как стресс, анестезия, биопсия опухоли. Все характерные для данной опухоли симптомы в этот период обостряются в связи с выбросом в кровь более значительных доз биологически активных веществ (гормонов).
Нейроэндокринные опухоли различных локализаций сопровождаются различными сочетаниями клинических проявлений. Среди общих признаков всех нейроэндокринных опухолей можно назвать кахексию (синдром проявляющийся отсутствием аппетита, тошнотой и снижением массы тела), энтеропатию (нарушение работы клеток стенки кишечника, сопровождающееся потерей белка и иногда отеками конечностей) и нефропатию (патология почек, сопровождающаяся значительной потерей белка с мочой, появлением отеков, преимущественно на лице, и повышением артериального давления).
Большинство нейроэндокринных опухолей ЖКТ – это нефункционирующие опухоли, клетки которых продуцируют биологически активные вещества, но при этом заболевание не сопровождается появлением типичных эндокринных синдромов.
Часто предъявляемые пациентом жалобы бывают обусловлены сопутствующими патологиями, однако в большей степени это касается нейроэндокринных опухолей желудка, среди которых можно выделить следующие типы:
- 1 тип – наиболее распространенный. Обычно не сопровождаются специфической эндокринной симптоматикой, а проявляются общими желудочными симптомами. Чаще встречаются у женщин в возрасте 50-60 лет.
- 2 тип – обычно возникает в рамках синдрома МЭН-2 (Синдром Сипла), может ассоциироваться с синдромом Золлингера-Элиссона. Встречается одинаково часто у женщин и мужчин, чаще в возрасте 50 лет.
- 3 тип – встречаются редко, данные опухоли не ассоциированы с какими-либо состояниями, могут длительное время не давать клинической симптоматики.
- 4 тип – встречаются редко, могут быть ассоциированы с МЭН-1 (Синдром Вермера), длительное время не проявляются какими-либо жалобами.
Нейроэндокринные опухоли поджелудочной железы в зависимости от тех клеток, из которых развиваются, сопровождаются различными проявлениями карциноидного синдрома:
- Гастриномы – опухоли из гастрин-продуцирующих клеток (могут встречаться в поджелудочной железе или других локализациях).
Обычно является частью синдрома Золлингера-Элиссона, который характеризуется наличием характерного комплекса симптомов: тяжелой рецидивирующей язвенной болезнью двенадцатиперстной кишки, гиперсекреторной активностью слизистой желудка и возникновением эндокринных гастрин-продуцирующих опухолей. Частой жалобой при наличии синдрома Золлингера-Элиссона также является диарея, которая в 10–20% случаев может являться ведущим клиническим симптомом. - Инсулиномы – опухоли из инсулин-продуцирующих клеток поджелудочной железы.
Для них характерна гиперинсулинемия и гипогликемический синдром (снижение концентрации глюкозы в крови), характеризующийся триадой Уиппла: развитие приступов спонтанной гипогликемии с потерей сознания натощак или после физической нагрузки; снижение содержания сахара крови (менее 2,2 ммоль/л) во время приступа; быстрое прекращение приступов внутривенной инъекцией глюкозы или приемом внутрь сахара. Гипогликемия сопровождается характерной симптоматикой: нарушениями сознания, нарушениями речи, головной болью, дезориентацией в пространстве и времени головокружением, общей слабостью, раздражительностью, нарушениями памяти, снижением остроты зрения, сонливостью, двоением в глазах, в очень тяжелых случаях – комой и судорогами. Тремор, тахикардия, беспокойство, бледность, повышенная потливость связаны с тем, что происходит возбуждение вегетативной нервной системы за счет избыточной секрецией катехоламинов. У многих пациентов наблюдается повышение массы тела вплоть до состояния ожирения, поскольку они постоянно испытывают чувство голода, вследствие чего возникает необходимость в частых приемах пищи. - Глюкагономы – это редко встречающиеся опухоли поджелудочной железы, чаще локализующиеся в ее хвосте. Эти опухоли растут медленно и сопровождаются неспецифическими симптомами. Для синдрома глюкагономы (синдром Маллисона) характерны некротическая мигрирующая эритема, глоссит, хейлит, развитие сахарного диабета, анемия, снижение массы тела, депрессия и тромбоз глубоких вен нижних конечностей.
- Соматостатиномы развиваются из клеток ПЖ, секретирующих соматостатин, встречаются очень редко. Эти опухоли обычно длительное время растут бессимптомно или со слабо выраженными неспецифическими симптомами. Для синдрома соматостатиномы характерно развитие сахарного диабета, снижение массы тела, холелитиаз (образование камней в желчных протоках), стеаторея («жирный стул») и гипохлоргидрия (сниженное содержание соляной кислоты в желудочном соке).
Нейроэндокринные опухоли кожи (Меркель-клеточная карцинома) представляют собой безболезненные плотные узлы, обычно возвышающиеся над уровнем кожи, имеющие красноватую окраску или сходные по цвету с окружающей кожей. Опухолевые узлы быстро растут и могут изъязвляться, при этом происходит образование сателлитов (дополнительных более мелких узлов на небольшом отдалении от первичного очага) и метастазирование опухоли. Типичной локализацией опухоли является лицо, голова и шея, несколько реже она встречается на конечностях, редко – на туловище, обычно в областях интенсивного воздействия солнечного света.
Нейроэндокринная опухоль надпочечников – феохромоцитома – характеризуется повышенной продукцией катехоламинов (адреналина, норадреналина, дофамина) и сопровождается характерным симптомом в виде значительного повышения артериального давления, плохо или вообще не поддающегося терапии антигипертензивными препаратами.
Диагностика нейроэндокринных опухолей
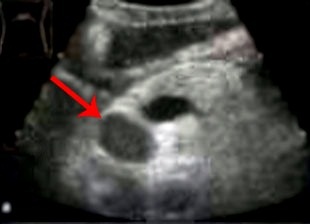 УЗИ. Опухоль головки поджелудочной железы
УЗИ. Опухоль головки поджелудочной железы 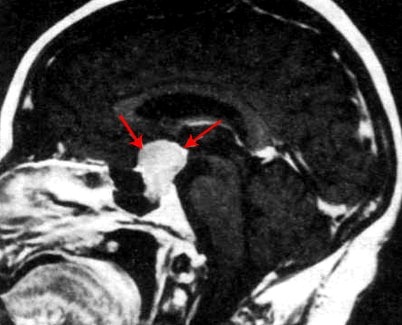 Рентгенограмма. Опухоль гипофиза
Рентгенограмма. Опухоль гипофиза
- Изучение личного и семейного анамнеза, а также наследственных заболеваний.
- Оценка клинического течения заболевания (жалоб пациента) и данных общего (физикального) осмотра.
- Лабораторные исследования. Особенностью нейроэндокринных опухолей является их способность секретировать различные гормоны и другие биологически активные субстанции – эти вещества являются специфическими маркерами для диагностики этих новообразований. Спектр основных маркеров включает:
- Хромотографин А – является общим маркером нейроэндокринных опухолей и обладает наилучшим сочетанием чувствительности и специфичности. Определение того белка является обязательной процедурой как для диагностики нейроэндокринных опухолей, так и для определения прогноза и контроля эффективности лечения.
- Уровень серотонина в крови и его метаболита – 5-оксииндолуксусная кислоты (5–ОИУК) – в моче. Эти вещества являются общими маркерами нейроэндокринных опухолей, используются для оценки биологической активности опухоли и карциноидного синдрома. Более информативным показателем является суточная экскреция 5–ОИУК.
- Другие общие маркеры: синаптофизин (маркер мелких везикул с нейротрансмиттерами), CD56 (маркер молекул нейроадгезии), NSE и PGP 9,5 (нейронспецифическая энолаза и протеин генного продукта 9,5 – маркеры цитоплазматических протеинов)
- При нейроэндокринных опухолях ЖКТ: гастрин, глюкагон, инсулин, проинсулин, С–пептид, панкреатический полипептид (ПП), вазоактивный интестинальный пептид (ВИП), соматостатин и гистамин.
- При нейроэндокринных опухолях легких: кальцитонин, гистамин, нейрон-специфическая енолаза (НСЕ), паратиреоидный гормон (ПТГ) и адренокортикотропный гормон (АКТГ).
- При феохромоцитоме: основные катехоламины (адреналин и норадреналин в крови или моче) и их метаболиты (экскреция с мочой нор– и метанефринов).
- При опухолях гипофиза: пролактин, лютеинизирующий гормон (ЛГ), фолликулостимулирующий гормон (ФСГ), тестостерон (у мужчин), эстрадиол (у женщин)
- При нейроэндокринных опухолях щитовидной железы: кальцитонин, тиреотропный гормон (ТТГ), трийодтиронин (Т3) и тетрайодтиронин (тироксин, Т4).
- При АКТГ–эктопическом синдроме: АКТГ и кортизол.
- Другие гормоны и пептиды при других локализациях.
- Биопсия пораженного органа с последующими исследованиями полученного материала:
- a. Гистологическое исследование – микроскопическое исследование материала, окрашенного специальными красителями для выявления патологических клеток.
- b. Иммуногистохимическое исследование – при этом исследуемый материал взаимодействует с реактивами, содержащими специфические белковые молекулы – антитела. При наличии в материале клеток с определенными структурами (антигенами) происходит их взаимодействие с антителами реактива, на основе чего выявляется опухолевая трансформация этих клеток.
- Функциональные нагрузочные тесты – применяются в диагностике нейроэндокринных опухолей ПЖ для исключения вторичного генеза гипогликемии и гиперинсулинемизма (клиническая симптоматика обусловленная относительным или абсолютным повышением содержания инсулина в крови).
- Ультразвуковое исследование (УЗИ), в том числе эндоскопическое (ЭУЗИ); компьютерная томография (КТ); магнитно-резонансная томография (МРТ), рентгенография. Используются для визуализации опухолевого очага в паренхиматозных органах (например, поджелудочной железе).
- Сцинтиграфия с аналогами соматостатина, меченными In-111. Нейроэндокринные опухоли содержат на своих клетках рецепторы соматостатина поэтому при введении аналогов соматостатина, меченных индием-111, происходит накопление того вещества в опухоли, и его избыточную концентрацию можно зарегистрировать с помощью компьютерной томографии.
- Наиболее современная методика диагностики: ПЭТ КТ с радиоактивным галием GA 68 ,соединенным с DOTA пептидами (GA 68 DOTA-TOC, GA 68 DOTA-TATE, GA 68 DOTA-NOC), обладающие высочайшей тропностью к соматостатиновыми рецепторам нейроэндокринных опухолей. Точность такого исследования достигает 100%.
Лечение нейроэндокринных опухолей
В лечении нейроэндокринных опухолей используются следующие подходы:
- Хирургическое лечение
- Биологическая терапия
- Химиотерапия
- Таргетная терапия, в том числе радионуклидная
- Радиотермоабляция
- Лучевая терапия
- Симптоматическое лечение
Хирургическое лечение
Оперативным методам отдается предпочтение на первых этапах лечения нейроэндокринных опухолей, при этом операция обычно совмещается с другими способами терапии в частности, радиоабляцией, эмболизацией и химиоэмболизацией.
Особенностями оперативного лечения Меркель-клеточной карциномы являются следующие:
- широкое иссечение опухолевого очага на коже с отступлением от краев опухоли как минимум 2 см и иссечением подлежащих тканей;
- использование специальных технологий для оценки чистоты краев резекции;
- одномоментная пластика раневого дефекта.
Биологическая терапия
Данный вид терапии помогает иммунной системе организма бороться с злокачественной опухолью. Производимые человеческим организмом или созданные искусственно вещества используются для стимуляции, усиления или воспроизведения эффектов противоопухолевого иммунитета организма. Также этот вид лечения называется биотерапией или иммунотерапией. Биологическая терапия нейроэндокринных опухолей проводится после оперативного лечения при определении низкого содержания маркера клеточной пролиферации Ki-67 (<3%), используются аналоги соматостатина (гормона роста человека), альфа-интерфероны, а также их комбинации. Кроме того, аналоги соматостатина также могут в случае умеренного (3–20%) и высокого (>20%) содержания Ki-67 при наличии клинического карциноидного синдрома для контроля симптомов.
Химиотерапия
Химиотерапия предполагает использование лекарственных препаратов для уничтожения раковых клеток, а также для угнетения их способности к делению. Химиотерапия нейроэндокринных опухолей проводится после оперативного лечения при определении умеренного (3–20%) и высокого (>20%) содержания Ki-67.
При лечении Меркель-клеточной опухоли химиотерапия назначается преимущественно при распространенном процессе либо при рецидиве заболевания.
Таргетная терапия
Таргетная терапия предполагает использование лекарственных препаратов или других веществ для идентификации и уничтожения раковых клеток посредством взаимодействия с имеющимися у них специфическими структурами (рецепторами), при этом не повреждая нормальные клетки, у которых эти рецепторы отсутствуют. В лечении нейроэндокринных опухолей данные препараты могут применяться на второй линии терапии.
Таргетная радионуклидная терапия
Данный метод заключается в применении радионуклидов (радиоактивных атомов), связанных с молекулой аналога соматостатина. Клетки нейроэндокринных опухолей содержат на себе большое количество рецепторов соматостатина, поэтому такие радионуклиды концентрируются в опухолевом очаге, и при их распаде энергия радиоактивного излучения воздействует только на клетки опухоли, не повреждая здоровые ткани.
Радиочастотная абляция (РЧА)
Данный метод лечения заключается в разрушении очагов патологической ткани посредством воздействия электрического тока высокой частоты. В лечении нейроэндокринных опухолей РЧА может применяться после оперативного лечения при определении умеренного содержания Ki-67 (3–20%).
Лучевая терапия
Данный метод лечения предполагает использование высоких доз лучевой энергии для уничтожения опухолевых клеток. Применяется в лечении Меркель-клеточной карциномы после операции для уничтожения оставшихся опухолевых клеток, а также при невозможности проведения оперативного лечения.
Симптоматическое лечение
При наличии функционирующих нейроэндокринных опухолей практически всегда возникают паранеопластические синдромы – состояния, обусловленные наличием опухоли и ее свойством продуцировать биологически активные вещества. Производится купирование беспокоящих пациента симптомов, при этом отсутствует влияние на причину из возникновения, поэтому данный метод терапии должен сочетаться с какими-то из вышеперечисленных.
В качестве примеров симптоматической терапии можно привести применение препаратов, снижающих секрецию соляной кислоты, при гастриноме, и гипотензивную терапию при феохромоцитоме.
Последующее наблюдение
После проведенного лечения нейроэндокринных опухолей рекомендуется прохождение регулярных осмотров для определения эффективности лечения, выявления побочных эффектов, а также своевременной диагностики рецидива заболевания. Во время осмотра производится тщательная оценка жалоб с выявлением динамики и исследование общих и специфичных биохимических маркеров в крови и моче.
Профилактика и скрининг
Профилактика и скрининг нейроэндокринных опухолей на данный момент не разработаны, поскольку эти новообразования не отличаются высокой частотой встречаемости.

