Лейкозами называют злокачественное разрастание незрелых клеток крови, чаще поражается лейкоцитарный росток, но в патологию вовлекаются и эритроциты, и тромбоциты. Лейкоз у детей составляет 1/3 от злокачественных опухолей.
Хронические формы заболевания в детском возрасте практически не встречаются.
Острый лейкоз у детей 2–3 лет чаще бывает лимфобластным. К нему более склонны мальчики с белой кожей (по сравнению с чернокожими и азиатами).
Миелоидная форма острого лейкоза обнаруживается еще раньше: в год, два – с одинаковой частотой среди мальчиков и девочек. В школьном возрасте симптомы болезни обнаруживаются редко.
Как происходит нормальное кроветворение?
Внутри костей имеется костный мозг. У грудничков он есть во всех костях, а к 15 годам — только в черепе, ребрах, позвонках, лопатках, тазовом скелете. Здесь расположены первичные стволовые клетки, из которых созревают эритроциты, лейкоциты и тромбоциты. Они отличаются от своих потомков по форме, наличию ядра, способности к делению и размножению. Но не могут выполнять «работу» зрелых клеток.
Спустя определенное время, нормальные клетки «доходят» до необходимого состояния и поступают в кровь готовыми к выполнению своих функций. В анализах очень редко попадаются единичные бластные (растущие) формы.
Какие клетки лежат в основе лейкоза?
2 разные формы острого лейкоза у детей отличаются по клеткам «виновникам» патологии:
- при лимфобластном лейкозе основными являются незрелые лимфоциты (лимфобласты);
- при миелоидной форме патология заболевание развивается за счет миелобластов, эритробластов, мегакариобластов и монобластов.
Причины
Поскольку лейкоз у детей развивается слишком рано (в этом возрасте человек редко встречается с факторами риска взрослых), то причины нужно искать в патологическом воздействии на плод во время беременности и в генетических мутациях.
Доказано влияние алкоголя и курения при беременности на возникновение миелоидного лейкоза крови ребенка.
К факторам риска со стороны матери также относятся:
- длительное пребывание на солнце;
- интоксикация ядовитыми продуктами на производстве (мышьяк, свинец, фосфорные соединения, бензин).
Наследственные заболевания, сопровождающиеся срывом иммунитета, включаются в факторы повышенного риска.
Значительно больше вероятность заболеть лейкозом выявлена у больных:
- с синдромом Дауна (в 15 раз);
- с синдромом Клинфельтера (дополнительная «х» хромосома у мальчиков, нарушающая развитие по мужскому типу);
- при анемии типа Франкони;
- при нейрофиброматозе и других редких заболеваниях.
Изучен риск заболеваемости в парах детей-близнецов:
- у однояйцевых близнецов при заболевании одного ребенка риск патологии для второго составляет 25%;
- у неоднояйцевых пар риск возрастает в 2–4 раза.
Проживание беременной женщины на территории, подвергшейся воздействию радиации, повышает риск лимфобластного лейкоза у ребенка в 5 раз, а миелоидного в 20 раз.
Проведение курса лучевой терапии с одновременным применением цитостатиков (Циклофосфан, Этопозид, Хлорамбуцил) при опухолях может привести в течение десятилетнего срока к опасному последствию в виде миелоидного острого лейкоза.
Повышен риск лимфобластного лейкоза у детей, получающих иммуноподавляющие препараты после трансплантации органов. Их вынуждены назначать для предупреждения отторжения.
Любые воздействия приводят к генетическим мутациям на уровне ДНК клеток костного мозга. Они начинают производить больше незрелых форменных элементов.
Клинические признаки
Симптомы лейкоза проявляются, когда нарушение кроветворения приводит к снижению нормальных дозревших форм клеток в периферической крови за счет их замены бластными формами.
Часто болезнь выявляется на фоне длительной инфекции: температура не снижается, антибиотики не помогают.
- ребенок слабеет, взрослые замечают его повышенную утомляемость при играх;
- кожа становится бледной, сухой;
- появляются носовые кровотечения, неожиданные синяки на теле;
- десны становятся рыхлыми и кровоточащими;
- боли в суставах и костях беспокоят 30% пациентов;
- ухудшается аппетит;
- появляются тупые боли в верхней части живота, вызванные увеличенной печенью и селезенкой, возможно увеличение живота;
- больного беспокоят головные боли, тошнота, рвота;
- снижается память и зрение — это проявления поражения головного и спинного мозга, они наблюдаются в 5–10% случаев;
- возникает сыпь на коже, изменяется цвет над участками высыпаний.
Эти симптомы вызваны «лишними» лейкоцитами, не способными защитить организм, снижением количества эритроцитов и тромбоцитов из-за угнетения их продукции.
Педиатр при осмотре обнаруживает увеличение лимфоузлов на шее, в подмышечной области, над ключицами, в паху.
Если увеличена вилочковая железа, она может сдавливать верхнюю полую вену. При этом происходит отек и посинение головы ребенка, беспокоит мучительный кашель, одышка.
Диагностика по крови
Диагностика начинается с исследования общего анализа крови. Лаборатория дает результат: увеличение лейкоцитов, недостаток тромбоцитов и эритроцитов, обнаружение молодых клеток.
При пункции подвздошной кости набирают небольшое количество костного мозга для исследования. Под микроскопом устанавливается процесс нарушенного кроветворения, подсчитываются бластные формы.
Биохимия крови позволяет оценить степень нарушения функции печени и почек.
Для изучения пораженности нервной системы берется пунктат спинного мозга, в нем находят проникшие бластные клетки. Подобным образом берется пунктат из лимфоузла.
Точный тип лейкоза устанавливается при исследовании в гематологическом отделении с помощью специального окрашивания.
Аппаратная диагностика
Некоторые методы применяются на поликлиническом этапе. Другие имеются только в специализированных клиниках.
- Цитометрия связана с пропусканием луча лазера через предварительно обработанную антителами кровь. Метод позволяет определить насыщенность клеток ДНК. Это важно для процесса лечения (такие клетки более чувствительны к лекарственным препаратам).
- Генетические исследования определяют поломку конкретной хромосомы, наследственный механизм передачи заболевания.
- При рентгенографии грудной клетки возможна диагностика увеличенных лимфоузлов в грудной и брюшной полостях, вилочковой железы. Этот признак подтверждается при магнитно-резонансной и компьютерной томографии.
- УЗИ помогает подтвердить увеличение печени и селезенки, крупных лимфоузлов.
- Сканирование костной ткани проводится для дифференциальной диагностики с опухолями костей, инфекционного воспаления, при неясном диагнозе.
Лечение
При выявлении лейкоза ребенка обязательно госпитализируют в специализированную клинику. Это может быть онкологическое или гематологическое отделения.
- уничтожить лейкозные клетки;
- поддержать иммунитет;
- предупредить возможное заражение инфекционными возбудителями;
- компенсировать недостаток эритроцитов и тромбоцитов.
Препараты цитостатического действия (химиотерапия) применяются в комбинациях для усиления эффекта.
Лучевая терапия назначается по показаниям для облучения головы.
Трансплантация костного мозга от донора проводится после применения высокодозной сочетанной терапии.
Каждому ребенку терапия подбирается индивидуально. Тактика определяется:
- факторами риска рецидива;
- массивностью бластных клеток;
- стадией поражения.
Назначенная терапия составляет целую программу, проходит определенные фазы. Такая терапия называется протоколом лечения. Существуют различные международные рекомендации (протоколы). Некоторые действуют около 20 лет. Важным отличием лечения по протоколу от обычной терапии других заболеваний является доказанный длительным применением четкий прогноз выживаемости.
Чем выше риск рецидива болезни, тем более интенсивным будет лечение.
Обычно курс терапии без трансплантации мозга длится около двух лет. За это время ребенка несколько раз кладут в стационар.
Этапы лечения
Протоколы планируют несколько этапов лечения:
- предварительный — начинается подготовка к основному курсу, состоит из короткого цикла химиотерапии с постепенным сокращением лейкозных клеток, предупреждаются нарушения почечной фильтрации продуктами распада клеток;
- индуктивный — интенсивная терапия несколькими препаратами, длится 5–8 недель, цель — достижение ремиссии;
- период консолидации с интенсивной терапией — закрепляет достигнутую ремиссию, предупреждает распространение на спинной и головной мозг, возможно применение облучения и введение цитостатиков в спинномозговой канал;
- повторная индукция — вводятся сильнодействующие комбинации препаратов курсами с перерывами, цель — «добить» бластные клетки, длительность от нескольких недель до месяцев;
- поддерживающая терапия — дозы препаратов невысокие, лечение амбулаторное, ребенку разрешается посещать садик или школу.
Протоколы помогают с каждым годом повышать результативность лечения детей. При этом накапливается опыт борьбы с осложнениями, побочным действием препаратов.
Прогностические факторы болезни
В ходе терапии острого лейкоза врач должен учитывать факторы, от которых зависит дальнейший прогноз. Считается, что они более важны для острого лимфоидного лейкоза.
Влияние факторов на степень риска рецидивов лимфоидного лейкоза показано в таблице.
Между «низким» и «высоким» рисками имеется еще группа стандартных показателей. Оценка риска как «очень высокого» включает сразу несколько пунктов.
При миелоидном лейкозе большую вероятность выздоровления имеют дети:
- с первоначальным лейкоцитозом менее 100000/мм3;
- с обнаруженными гранулами-включениями внутри клеток;
- страдающие синдромом Дауна;
- имеющие положительные сдвиги после одного лечебного цикла.
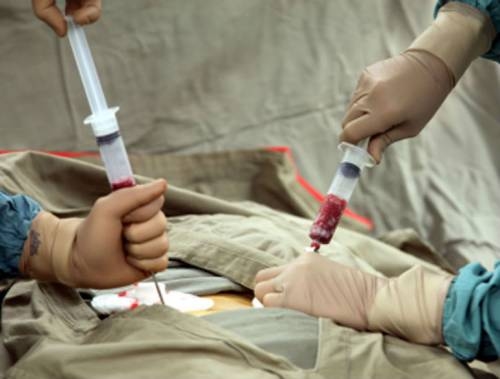
Операции по трансплантации костного мозга позволяют спасать жизнь пациентам
Прогноз жизни
Для детей с лимфобластной формой острого лейкоза вероятность излечения:
- при низком риске — 85–95%;
- при стандартном — 65–85;
- при высоком — 60–65%.
Пятилетняя выживаемость в настоящее время — 85%.
Дети с миелоидным острым лейкозом имеют следующие шансы:
- при стандартной терапии выздоравливают 40–50% пациентов;
- при трансплантации костного мозга от кровных родственников — 55–60%.
Пятилетняя выживаемость – до 45% случаев.
Постоянно проводятся крупные международные исследования по лечению лейкозов. Пациентам следует выполнять существующие протоколы лечения и надеяться на новые лекарственные препараты.

