Долечебная клиническая классификация TNM
- Т — Первичная опухоль
- TiS Преинвазивная карцинома (carcinoma in situ)
- ТО Первичная опухоль не определяется
- Т1 Опухоль находится в пределах губы: 2 см или менее в наибольшем измерении
- Т2 Опухоль находится в пределах губы: больше 2 см. но не больше 4 см в наибольшем измерении
- ТЗ Опухоль находится в пределах губы: больше 4 см в наибольшем измерении
- Т4 Опухоль распространяется на соседние органы: кость, язык, кожу шеи и т. д.
- ТХ Определить в полной мере распространенность первичной опухоли невозможно
- N — Регионарные лимфатические узлы
- N0 Регионарные лимфатические узлы не пальпируются
- N1 Пальпируются смещаемые лимфатические узлы на стороне поражения
- N2 Пальпируются смещаемые лимфатические узлы на противоположной или с обеих сторон
- N3 Пальпируются несмещаемые лимфатические узлы
- NX Оценить состояние лимфатических узлов невозможно
- М — Отдаленные метастазы
- М0 Признаков отдаленных метастазов нет
- M1 Отдаленные метастазы определяются
- MX Определить отдаленные метастазы невозможно
Послехирургическая гистопатологическая классификация pTNM
- рТ — Первичная опухоль
- рТ категории являются аналогичными Т категориям
- pN — Регионарные лимфатические узлы
- pN категории являются аналогичными N категориям
- рМ — Отдаленные метастазы
- рМ категории являются аналогичными М категориям
Группировка по стадиям
- Т1
- Т2>2 см — 4 см в пределах губы
- Т3>4 см
- Т4 Распространяется на другие органы
- N1 Смещаемые лимфатические узлы на стороне поражения
- N2 Смещаемые лимфатические узлы на противоположной стороне или с обеих сторон
- N3 Несмещаемые лимфатические узлы
Диагностика. Описанные выше основные признаки рака губы позволяют в большинстве случаев правильно поставить диагноз. При этом следует учесть существовавшие ранее предопухолевые изменения слизистой оболочки, такие моменты, как периодическая смена роговых корочек, увеличение изъязвления, кровоточивость, безболезненное уплотнение краев и основания язвы.
Существенную помощь в дифференциальной диагностике воспалительных предопухолевых процессов и рака губы могут оказать стоматоскопия, хейлоскопия. На важность использования этого метода неоднократно указывали в конце 60-х годов и позже А. А. Кунин, И. И. Ермолаев и др. Однако в практику метод хейлоскопии почему-то не внедряется, хотя улучшает раннюю диагностику рака губы. В 1979 г. завершена работа М. Д. Филюрина, проводившего хейлоскопическое, хейломикроскопическое и цитологическое исследования для диагностики предопухолевых процессов и рака губы. Автор, так же как и его предшественники, высоко оценивает диагностическое значение перечисленных методов, особенно их комплексное использование. Нужно согласиться с мнением М. Д. Филюрина, что хейлоскопия должна шире применяться на первом этапе обследования. Хейлоскопическая картина рака губы при ранней стадии характеризуется наличием валика, кровоточивостью, грубым рельефом ткани, отсутствием реакции атипичных сосудов на сосудосуживающие вещества, резкой йод отрицательной пробой Шиллера — Писарева и интенсивным окрашиванием глубоких участков ядерной краской. При воспалительных и предопухолевых процессах хейлоскопическая картина иная и перечисленные признаки отсутствуют или выражены слабо.
В неясных случаях сомнения могут быть разрешены цитологическими исследованиями отпечатков, пунктатов и биопсийного материала. Клинический опыт показывает, что биопсия не вызывает осложнений. Ее проводят после инфильтрации намеченного участка губы 0,5% раствором новокаина. Из края опухоли или язвы иссекают кусочек ткани размером 5—8 мм, захватывая участок здоровой ткани. Иногда с целью гемостаза рану смазывают раствором карболовой кислоты или производят поверхностную электрокоагуляцию. При развитых формах рака губы диагностических затруднений обычно не бывает. Крайне редко приходится дифференцировать с туберкулезной гранулемой и сифилитической язвой.
Лечение. При раке губы лечение должно строиться с учетом стадии процесса и клинической формы. Ведущим и наиболее результативным оказался комбинированный метод лечения, который слагается из двух этапов: излечения опухолевого очага на губе и удаления шейной клетчатки. Перед лечением больные должны бросить курить, пройти санацию полости рта.
Лечение рака губы I стадии (первичного опухолевого очага) можно осуществить хирургическим или лучевым способом. В настоящее время очень редко применяется оперативный метод. Он состоит в следующем: отступя от края инфильтрации на 1,5—2 см, производят квадратную или трапециевидную (но не клиновидную) резекцию губы. Изъяны нижней и верхней губы могут быть закрыты путем операций Брунса или Мальгеня.
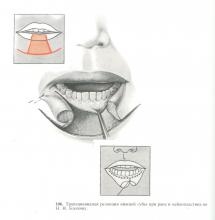
Мы считаем, что более радикальным является иссечение трапециевидного участка губы, расширяющегося книзу. Более косметическим следует считать закрытие изъяна по Н. Н. Блохину (рис. 106).
Чаще используют лучевой метод: внутритканевое введение радиоактивных игл или короткофокусную рентгенотерапию. Последний вид лечения благодаря хорошим отдаленным и косметическим результатам стал методом выбора. По утверждению некоторых авторов, при лечении рака губы I стадии этим методом можно добиться почти 100% излечения. Короткофокусная рентгенотерапия проводится на различных аппаратах (РУМ-7, ТУР-60, РТ-100), работающих при генерировании напряжения рентгеновской трубки 60—100 кВ. Поля облучения располагаются со стороны красной каймы и кожи нижней губы. Суммарная очаговая доза составляет обычно 6000 рад (60 Гр) при разовой дозе 400—500 рад (4—5 Гр).
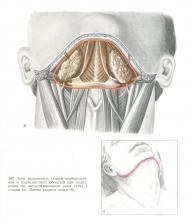
Вопрос о регионарных лимфатических узлах можно решать только после излечения первичного опухолевого очага. Большинство онкологов при раке губы I стадии не удаляют их. В подобных случаях, особенно у ослабленных больных и стариков, следует установить динамическое наблюдение. Однако некоторые хирурги считают, что удаление подчелюстных и подбородочных лимфатических узлов следует производить при всех стадиях рака губы. Мы считаем, что при подозрении на метастазы в регионарных лимфатических узлах необходимо сделать цитологическое исследование пунктата узла. При подтверждении диагноза метастазирования осуществляется фасциально-футлярное иссечение клетчатки подчелюстных и подбородочной областей вместе с поверхностной мышцей шеи. Эта операция хорошо разработана Н. А. Тищенко. На рис. 107 показана зона тканей, которую мы обычно удаляем при типичной операции Банаха (только при раке нижней губы I стадии).
Лечение рака губы II стадии в большинстве случаев осуществляется лучевыми методами. При локализации очага ближе к углу рта показана глубокая, ближе к середине — близкофокусная рентгенотерапия. При отсутствии аппарата для близкофокусной рентгенотерапии можно использовать близкофокусные гамма-терапевтические установки. Спустя 2—3 нед после окончания лучевого лечения первичного очага производится верхнее фасциально-футлярное иссечение шейной клетчатки: удаление клетчатки подбородочной и подчелюстных областей с одновременным иссечением глубоких шейных узлов в области развилки общей сонной артерии и лимфатических узлов нижнего полюса околоушной слюнной железы. Описанное оперативное вмешательство следует производить очень тщательно. К операции можно приступать после излечения первичной опухоли, причем ее следует производить при прощупываемых и не прощупываемых метастазах. Обусловлено это тем, что клинические методы установления регионарных метастазов, а также обычные гистологические методы не всегда являются достоверными. Как показали А. И. Савицкий и М. К. Куланбаев (1964), для точного диагноза нужны гистологические исследования ступенчатых срезов.
При раке губы III стадии лечение первичной опухоли проводится сочетанным лучевым методом. При этом обычно используется облучение на гамма-терапевтических установках, заряженных радиоактивным кобальтом 60 Со. При отсутствии указанного аппарата можно применить близкофокусную рентгенотерапию (напряжение генерирования трубки 70—120 кВ) в сочетании с контактным облучением остатка опухоли. Если опухоль сильно уменьшилась, но не подверглась полной регрессии, то показано внедрение в ложе опухоли радиоактивных препаратов. Остатки неизлеченной опухоли удаляют путем квадратной резекции губы. Однако очень часто трудно установить сроки иссечения остатков неизлеченной опухоли после окончания облучения. Обычно эти сроки составляют 3—6 нед, но иногда клиническое течение регрессии опухоли не позволяет даже по прошествии 1,5 мес определить срок оперативного вмешательства. Вопрос о сроках операции должен решаться в процессе динамического наблюдения, когда полностью реализован лучевой эффект в тканях: стихли реактивные явления и закончилась регрессия опухоли.
Второй этап лечения — удаление шейной клетчатки — осуществляется после полной регрессии первичной опухоли. Если до лучевого лечения имел место рак III стадии, то следует произвести фасциально-футлярное иссечение шейной клетчатки с обеих сторон одномоментно. У пожилых и ослабленных больных эту операцию можно сделать сначала с одной стороны, а через 2—3 нед — с другой. При наличии в регионарных лимфатических узлах метастазов операции предшествует предоперационная дистанционная гамма-терапия, которая должна осуществляться параллельно с лучевой терапией первичной опухоли. Дистанционная гамма-терапия на область метастазов способствует уменьшению метастатических узлов и развитию в них дистрофических изменений (суммарная очаговая доза 3000—4000 рад, или 30—40 Гр). При спаянии метастазов с внутренней яремной веной показано иссечение шейной клетчатки по Крайлу.
Исключительно сложно лечить местно распространенную форму рака губы (IV стадия). В отдельных случаях в сочетании с противовоспалительным лечением может быть произведена близкофокусная гамма-терапия. Некоторые радиологи в таких случаях предлагают перед облучением перевязывать наружные сонные артерии, что якобы повышает эффект лучевого воздействия. После облучения при показаниях иногда может быть осуществлена широкая электроэксцизия опухоли с резекцией нижней челюсти. В последующем производят пластические операции для восстановления губы, подбородка, щеки. Проведение и правильная оценка лучевого лечения местно распространенных форм рака губы, широкие оперативные вмешательства и последующие восстановительные операции — все эти сложные вопросы могут решаться только при совместной работе нескольких высококвалифицированных специалистов.
Регионарная химиотерапия колхамином, сарколизином и другими препаратами при первичном и рецидивном местно распространенном раке губы не получила практического применения. Использование системной химиотерапии показало, по данным нашей клиники, что современные противоопухолевые препараты при раке губы не эффективны. Лишь метотрексат в отдельных случаях оказался полезным при лечении преимущественно первичного очага рака губы. Метастазы рака губы в регионарных лимфатических узлах малочувствительны к метотрексату, однако крайне редко они под влиянием метотрексата подвергаются частичной регрессии. По литературным данным, сочетание метотрексата с лучевой терапией позволяет улучшить результаты лечения.
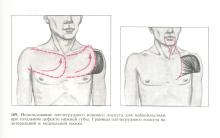
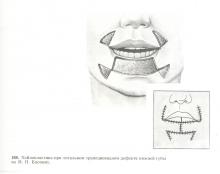
При рецидиве рака губы лечение осуществляется в зависимости от размеров опухоли, формы роста и состояния окружающих опухоль здоровых тканей. При небольших опухолях после лучевой терапии производится электроэксцизия губы в пределах здоровых тканей с последующей пластикой местными тканями. При больших дефектах используются различные методики восстановления губы: по Н. Н. Блохину (1941), Ф. Л. Гектину (1940), кожным плечегрудным лоскутом (рис. 108, 109), пластика стеблем Филатова и т. д. При больших опухолях и отсутствии раковых изменений кожи может быть осуществлена дистанционная гамма-терапия.
Рецидив рака губы можно лечить также методом внутритканевой бета-гамма-терапии полых нитей, метод разработан А. С. Павловым. Регионарные рецидивы (вторичные метастазы) представляют большие трудности для лечения, они резистентны к лучевому лечению, поэтому при одиночных подвижных метастазах показано их удаление, при множественных и малосмещаемых — паллиативная гамма-терапия, иногда до пределов выносливости тканей. Через 2—4 нед после завершения лучевой терапии решается вопрос об операбельности регионарного рецидива и о характере операции.
Прогноз зависит от распространенности рака губы, своевременности лечения и опыта онколога. На результаты лечения во многом влияют оценка распространенности опухолевого процесса и метод, который впервые был использован. В общем прогноз можно считать более благоприятным, чем при злокачественных опухолях органов полости рта и верхних дыхательных путей. Объясняется это прежде всего локальностью процесса, что значительно облегчает лечение. Однако прогноз резко ухудшается при появлении множественных регионарных метастазов. Трудоспособность после излечения в большинстве случаев восстанавливается, но нередко больному приходится менять прежнюю работу на открытом воздухе на работу в других условиях.
Стойкое излечение при раке нижней губы достигается в 60—70% случаев. Такие результаты "Касаются преимущественно больных с распространенностью злокачественной опухоли I — II стадии. При раке нижней губы III стадии отдаленные результаты значительно хуже — пятилетняя выживаемость составляет 30—40%. При множественных и двусторонних регионарных метастазах стойкое излечение наблюдается редко. Особенно плохой прогноз в тех случаях, когда отдельные метастазы на шее прорастают в кожу и клинически напоминают кистозный процесс.
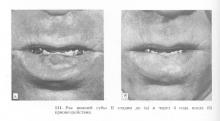
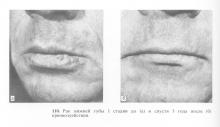
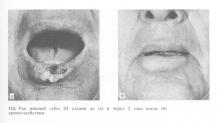
Отдельно следует остановиться на исследованиях криогенного метода лечения рака губы, проводившихся в нашей клинике на протяжении 70-х годов. Лечению подверглось более 170 больных с различными стадиями опухолевого процесса. Больные с опухолями I и II стадии составили группу в 97 человек. Отдаленные результаты изучены на протяжении 5 лет и более — здоровыми оказались 97% человек (рис. 110, 111), причем с хорошим функциональным исходом. У 3,4% больных после излечения первичного очага криовоздействием развились одиночные регионарные метастазы, по поводу чего произведены соответствующие операции. В группе больных раком губы III стадии было 27 человек; через 5 лет и более здоровы 67% (рис. 112, 113).
Регионарные метастазы развились у 12% больных — они были оперированы.
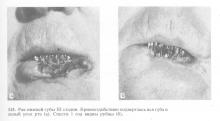
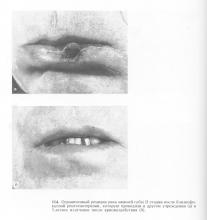
Хорошие результаты были достигнуты также при использовании криогенного метода у больных с ограниченными рецидивами и радиорезистентными опухолями (22 больных) — здоровы 80% (рис. 114). Больные с распространенными раковыми опухолями нижней губы, в том числе рецидивными, составили группу в 55 человек, через 5 лет были живы 55%. При распространении опухолевого процесса на нижнюю челюсть, но без разрушения ее, методом криовоздействия можно осуществить радикальное вмешательство и сохранить целостность нижней челюсти. При опухолях губы с регионарными метастазами криовоздействие на первичный опухолевый очаг можно производить одномоментно с иссечением шейной клетчатки. Примерно такие же результаты лечения больных раком нижней губы криовоздействием сообщают Л. И. Трушкевич и соавт. (1976).
В заключение следует подчеркнуть, что анализ результатов и методики криовоздействия резко изменили наши представления о лечении больных раком губы. Мы считаем, что этот метод является методом выбора при лечении первичного опухолевого очага I, II и III стадии, ограниченного рецидива. При распространенных процессах вопрос о использовании этого метода следует решать применительно к конкретному больному. После криогенного лечения за больным нужно установить периодическое наблюдение и в случае развития регионарного метастазирования произвести удаление шейной клетчатки.
Таким образом, длительное локальное развитие рака губы без явной тенденции к регионарному метастазированию и развитию отдаленных метастазов, возможность ежедневного осмотра губы и раннего диагностирования опухоли, наличие эффективных методов лечения позволяют надеяться, что практически большинство больных раком губы должно быть излечено. В наше время рак губы не должен быть причиной смерти.

